Anvisa libera retomada dos testes da Coronavac
Agência tomou a decisão após receber novos dados do Instituto Butantan que mostram que morte de voluntário não tem relação com a vacina
Publicado: 11 Novembro, 2020 - 15h20
Escrito por: Tiago Pereira, da RBA
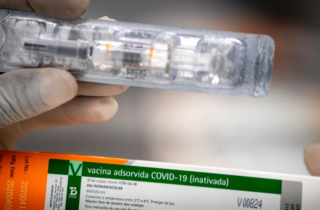
A Agência Nacional de Vigilância Sanitária (Anvisa) autorizou nesta quarta-feira (11) a retomada dos testes clínicos da vacina Coronavac. O órgão explica que tomou a decisão após receber do Instituto Butantan, de São Paulo, novos dados que mostram que o “evento adverso grave (EAG)”, que culminou na morte de um voluntário, não tem relação com a vacina.
Em nota, a Anvisa disse que agora “tem subsídios suficientes para permitir a retomada da vacinação”. Também afirma que segue acompanhando o desfecho do caso que determinou a suspensão.
A agência diz que foi informada da causa da morte em reunião com representantes do Butantan na manhã desta terça, e depois comunicada oficialmente na parte da tarde. Também receberam Boletim de Ocorrência que aponta o suicídio do voluntário como a principal hipótese investigada.
Além disso, a Anvisa também recebeu parecer do Comitê Internacional Independente que corrobora com as informações prestadas pelo instituto paulista. Esse documento do comitê já recomendava a retomada dos estudos.
Ainda nesta terça, os representantes da Anvisa haviam alegado que o Instituto Butantan teria repassado “informações insuficientes e incompletas”, sem especificar a causa do óbito. O laboratório paulista negou que faltassem dados, mas enviou nova comunicação à agência no final da tarde.
A Anvisa voltou a defender como “adequada” a decisão tomada na segunda-feira (9) que paralisou dos estudos da Coronavac. “A medida, de caráter exclusivamente técnico, levou em consideração os dados que eram do conhecimento da Anvisa até aquele momento”.
Por outro lado, o órgão também destaca que a suspensão e retomada de estudos clínicos são “episódios comuns em pesquisas clínicas”. Contudo, alegam que esse tipo de decisão “não significa necessariamente que o produto sob investigação não tenha qualidade, segurança ou eficácia”.


